时间:

作者:陈谕园、吴松、陈丽青、张媛媛、高钟镐、李天磊、黄伟、杨庆云
翻译:华溶应用中心
地拉罗司是治疗成人和儿童地中海贫血引起的铁超负荷的一线药物。其在生物药剂学分类系统中被分类为II类化合物,因此在制造过程中应严格控制其活性药物成分 (API) 的粒度。本研究采用激光衍射法测定地拉罗司原料药的粒度分布。我们还通过研究重要的光学参数和样品分散条件,开发并验证了一种准确且方便的方法。相对标准偏差值,即d (0.1),d (0.5) 、d (0.9) 和d (4,3),通过方法学验证和实际样品测量测得的值< 3%。比较了不同粒径地拉罗司制备的几批分散片在4种溶出介质中的溶出曲线,考察了粒径对药物体外溶出的影响。结果表明,地拉罗司原料药的粒度分布显著影响其分散片的释放。
作为一种遗传性疾病,地中海贫血可归因于血红蛋白产生紊乱,在地中海地区的人群中尤其常见。铁过载是地中海贫血的主要症状之一。人体不能去除多余的铁。因此,目前可用的铁螯合剂,例如去铁酮和去铁罗司,用于处理各种疾病中的铁过载。地拉罗司属于三齿铁螯合剂,其中两个地拉罗司分子与每个铁(Fe3+原子形成稳定的复合物(图1A)。与其他铁螯合剂相比,该螯合剂具有安全性和有效性方面的优势。虽然肾毒性是地拉罗司的严重不良反应,但此药广泛用于治疗成人和儿童输血含铁血黄素沉着症。Deferasirox分散片(以Exjade ®上市)已于2005年被食品和药物管理局(FDA)批准为一线疗法,于2006年被欧洲药品管理局(EMA)批准为一线疗法。此外,地拉罗司于2002年3月被EMA指定为孤儿药。
地拉罗司的活性成分是白色至灰白色结晶性粉末。该粉末易溶于二甲基甲酰胺和二甲基亚砜,微溶于甲醇,几乎不溶于水。颗粒大小和分布差水溶性药物直接影响其在体内的释放和吸收及其疗效。通常,小微粒具有可用于扩散的大表面,增加释放速率。因此,在生产地拉罗司分散片时,应严格控制粒度分布。本品粒度的质量控制应建立准确方便的测量方法。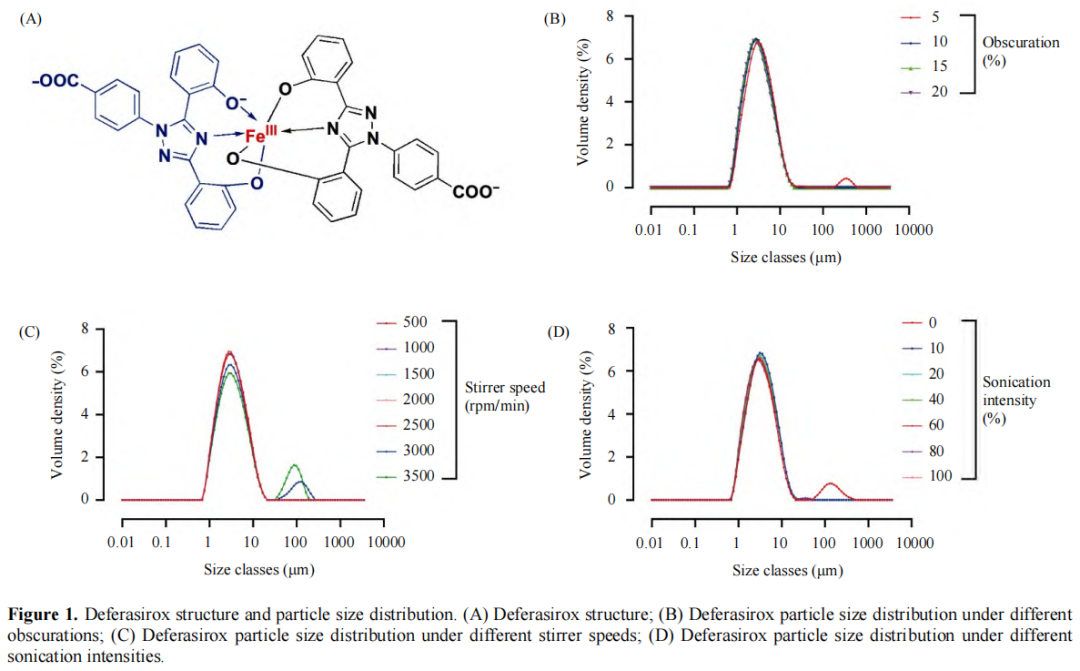
迄今为止,用于评估微粒尺寸的常用技术包括光学显微镜、沉淀、扫描电子显微镜 (SEM) 、筛析和激光衍射方法。光学显微镜的优点是可见性。然而,该方法的主要缺点是耗时的手动样品制备。SEM具有类似的缺点,它主要用于表征微粒的内部结构和表面形态。沉降试验时间方法长,操作复杂。虽然筛分分析因其成本低而被广泛使用,但尺寸小于38 μm的干粉难以测量。此外,结果受到人为因素的显著影响。
激光衍射是一种基于Mie理论和Fraunhofer近似的测量方法。该方法通过测量散射光强度的空间分布来确定粒子的尺寸和分布。激光衍射具有良好的重复性和精确性,近年来在材料科学和药剂学研究中得到了广泛的应用。然而,尚未报道用于测量地拉罗司活性药物成分 (API) 的粒度和分布的可用激光衍射方法。在目前的研究中,使用激光粒度分析仪MalvernMastersizer 3000来研究地拉罗司粒度测量的关键影响因素。讨论了尺寸测量程序的发展,并系统地验证了最佳激光衍射方法。使用该方法准确测定了几批API样品的粒度和分布。用体积平均粒径d (4,3) 表征颗粒的尺寸差异。粒度分布由d (0.1) 、d (0.5) 和d (0.9) 表征。此外,在4种溶出介质中比较了不同粒径地拉罗司制备的几批分散片的溶出特性,研究了粒径对药物体外溶出的影响。
2.1材料
大量地拉罗司原料药(批号20180201、20180202、20180203和20190523)在我们的合成实验室(中国北京)生产。地拉罗司分散片(批号20180622、20180629和20191209)也在我们的制药实验室(中国北京)生产。商业分散片(批号SP168)购自诺华公司制药公司SteinAg(瑞士巴塞尔)。地拉罗司参比物质从美国药典获得。聚山梨酯80 (Tween-80) 由阿法埃莎 (中国天津)提供。阿拉丁(中国上海)提供约10%壬基酚乙氧基化物 (NP-40) 水溶液。质量审计标准颗粒从摩文分析有限公司购买。(英国伍斯特郡马尔文)。高效液相色谱 (HPLC) 级乙腈 (ACN) 和甲醇 (MEOH) 来自西格玛奥德里奇公司 (St.用于制备流动相.用MilliQ系统纯化去离子水(Millipors,比勒利卡.MA,美国),自制,采用0.22μm过滤膜过滤。除非另有说明,其他化学品均为分析级。
2.2仪器仪表
使用激光衍射粒度分析仪(粒度分析仪 3000,马尔文仪器有限公司.,伍斯特郡英国)用600 mL悬浮烧杯测量地拉罗克斯原料药的粒度分布。采用以下优化参数进行测量:颗粒折射率,1.699;颗粒吸收指数,0.1;中等折射率,1.330;样品测量持续时间,5s;背景测量持续时间,5s;测量次数,3次;和测量之间的延迟,5s。将测量装置的搅拌器速度设定为2500 r/min以防止样品悬浮液的沉降。在样品测量之间,将分散单元排出并用去离子水洗涤。使用弗劳恩霍夫模型、通用分析模式和假设不规则粒子形状,使用马尔文马斯特西策3000软件(版本3.40)分析马斯特西策原始数据。
使用自动溶出仪 (推荐使用华溶DS-1206AT全自动取样溶出系统) 和TU-1810 DPC紫外 (UV) -可见分光光度计 (Perview,China,China) 测试地拉罗司分散片的溶出曲线。在285纳米波长下测量吸光度。
安捷伦1260液相色谱系统,配有分光光度二极管阵列检测器。美国加利福尼亚州圣克拉拉)用于测定溶解度。Inertsil ® ODS-3柱(150 mm×3.0 mm,3um粒径;GL科学公司,日本)在15 ℃的烘箱温度下操作以进行分离。流动相A是磷酸二氢钾的20 mM水溶液。
预先调节至pH值2.5,流动相B为乙腈。流动相A和B以48∶52 (v/v) 的比例混合。流速保持在0.5 ml/min,注射体积为10ul,并且在245纳米进行紫外检测。
2.3粒度分析
称取样品(25mg地拉罗司),置于50ml锥形瓶中。随后,加入40 ml分散剂(0.1% NP-40在水中),并充分振摇混合物。将混合物在室温下超声处理8分钟,然后用分散剂稀释体积以获得悬浮液。向预充有去离子水的600 ml烧杯中加入约2ml的样品体积。添加另外的样品直到达到10%和15%之间的遮蔽水平。分散单元中的搅拌器速度设定为2500 r/min,内部超声处理40%。每个样品至少进行三次测量。
2.4溶解度测定
制备浓度为0.06%、0.1%、0.3%、0.6%和0.9%的100 mL的NP-40水溶液。5个地拉罗司API(批号20180201)称量约25mg/剂,并置于不同浓度的NP-40水溶液中。通过超声处理将样品完全悬浮并用0.22um膜过滤。此后,将随后的滤液用作样品溶液。准确称取约25mg地拉罗司参比物质并转移至25- ml容量瓶中。用10 ml甲醇填充烧瓶并超声处理约15min以溶解参比物质。然后用50%乙腈-水稀释至刻度。随后,用50%乙腈-水将1.0 ml该溶液稀释至50ml,并且摇匀,得到标准溶液。对样品和标准溶液进行HPLC分析。使用等式 (1) 计算不同浓度下地拉罗司在NP-40水溶液中的溶解度:

其中Ax和As分别是来自样品和标准溶液的峰值响应;ms是地拉罗司标准的加权质量;Vs是标准溶液的稀释倍数。
2.5溶出介质的制备方法
简言之,0.5%吐温20水溶液,0.5%使用Tween-20 pH 6.8磷酸盐缓冲溶液、0.5% Tween-20 pH 4.5醋酸盐缓冲溶液和0.5% Tween-20 pH 1.0盐酸溶液作为溶解介质。这些培养基制备如下。
对于0.5%吐温- 20水溶液:称取5g吐温20,溶于1000 ml水中。
对于0.5% Tween-20 pH 6.8磷酸盐缓冲溶液:称取6.8045克磷酸二氢钾和0.896克氢氧化钠,溶于适量水中。然后用水将溶液稀释至1000 ml。随后,加入5g吐温20并完全溶解。
对于0.5% Tween-20 pH 4.5醋酸盐缓冲溶液:称取2.99g乙酸钠,向其中加入1.6 ml冰醋酸,用水稀释至1000 ml。随后,加入5g吐温- 20并完全溶解。
对于0.5% Tween-20 pH 1.0盐酸溶液:用水将9ml盐酸稀释至1000 ml。然后,加入5g吐温20并完全溶解。
2.6溶出曲线测定方法
采用中国药典溶出试验的第二种方法,取上述溶出介质测量溶出曲线。中位体积为900 ml。转速为50r/min,中值温度为37±0.5℃。在5min、10min、15min、20min、30min、45min和60min取约5min的溶出介质。此后,补充5 ml的溶解介质。精确地,将4ml该溶液与4ml乙腈混合并用作样品溶液。准确称取一份地拉罗司参比物质,并以25ug/ml乙腈稀释。精确地,将5ml该溶液与5ml溶解介质混合并用作标准溶液。还进行了紫外-可见分光光度法。使用等式 (2) 计算不同时间点的累积释放百分比,并绘制溶解曲线: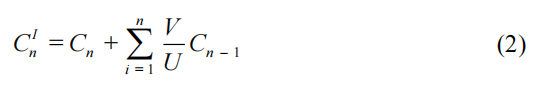
式中Cn和CnI分别为采样的实测值和校正值;U和V分别为总采样体积和采样体积。 采用相似因子(f2)比较不同粒径的去甲恶灵分散片与参比分散片的溶出度分布: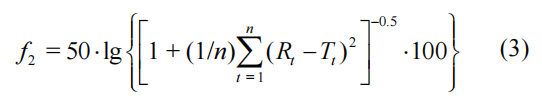
其中n为数据点数;Rt和Tt分别为参比制剂和被测制剂在特定时间点的溶解百分比。如果f2≥50,则认为溶出度分布相似。
3.1分散剂的选择
地拉罗司易溶于二甲基甲酰胺和二甲基亚砜,但不溶于水。从分散剂选择的原则出发,综合考虑经济、无毒、环保等方面的优势,将水作为测定地拉罗司粒径的分散介质。然而,地拉罗司是疏水性的,并且在与水接触或漂浮在液体表面上时表现出明显的聚集倾向。表面活性剂可用于“湿润”地拉罗司晶体并减少聚集。通过添加适当的分散剂,随着表面张力降低,亲水性增加得到加强。采用外部超声搅拌,有效地减少了悬浮液的聚集,提高了悬浮液的稳定性。该方法能够均匀稳定地通过光学检测单元并获得精确的粒径和分布结果。
本研究考察了0.1% Tween-80和0.1% NP-40两种分散剂水溶液对样品的分散性。结果表明,以0.1%吐温-80水溶液为分散剂时,样品的分散稳定性较差。样品粉末表现出聚集和沉淀现象。多次并行测量的精度较差。以0.1%的NP-40水溶液为分散剂时,样品的稳定性较好。超声处理后样品仍能均匀分散。测量结果令人满意,具有良好的精度。因此,采用0.1%的NP-40水溶液作为分散剂,测量地拉罗司的粒径和分布。
3.2分散剂浓度的研究
制备不同浓度的NP-40水溶液,例如0.06%、0.1%、0.3%、0.6%和0.9%。称取每剂约25 mg的5个地拉罗司API,并置于不同浓度的NP-40水溶液中。此后,测定样品溶液的粒度和溶解度。每个样品至少进行三次测量。利用d (0.1) 、d (0.5) 、d (0.9) 和d (4,3) 的平均值研究分散剂浓度对测量结果的影响;相对标准偏差(RSD %);加权残差作为调查指标(补充A)。还进行了HPLC(如补充数据中附录B所示)。计算了不同浓度的NP-40水溶液中地拉罗司的溶解度。表1提供了测量结果。
表1中的结果表明,基于差的分散均匀性和RSD %值,当分散剂浓度<0.1%时,样品溶液不完全分散。随着NP-40浓度的逐渐增加,地拉罗司颗粒尺寸的测量结果趋于稳定。当分散剂中的浓度达到0.3%时,地拉罗司的溶解度显著增加,导致小尺寸的严重损失。因此,综合考虑了0.1% NP-40。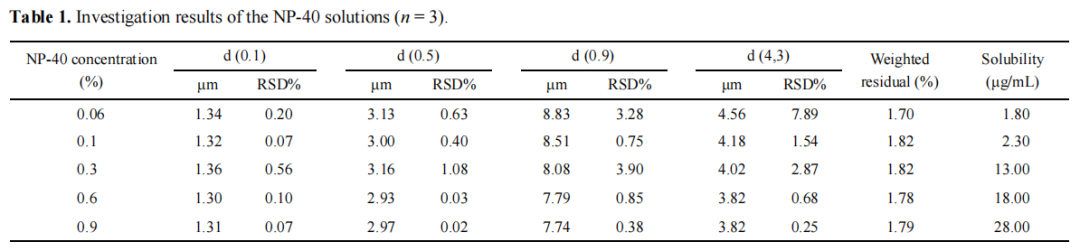
3.3光学参数的研究
颗粒尺寸测量的重要光学参数包括介质折射率、颗粒折射率、颗粒吸收指数和遮蔽度。介质为水,其折射率为1.330。地拉罗司的折光率和吸光率分别为1.669和0.1。遮蔽也是一个关键的光学参数,可以直接反映样品量。如果遮蔽太高或太低,则由于颗粒的多次散射和测量结果的差的代表性,颗粒尺寸和样品分布将受到影响。在本研究中,我们研究了不同遮蔽对颗粒尺寸测量的影响。结果见表2和图1B(补充C)。表和图显示遮蔽在10% -20%范围内。测量结果、精度和残差均令人满意。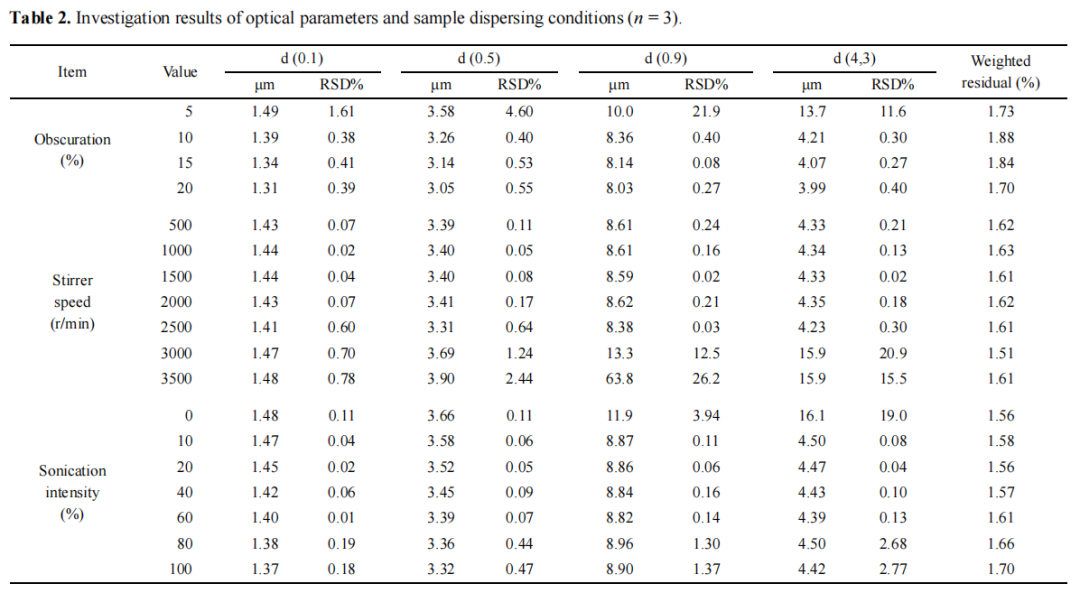
3.4样品分散条件的研究
粒度测量的重要光学参数是介质折射率和颗粒。Deferasirox API由于其尺寸小,易于在水中聚集。合适的搅拌器速度和超声处理方法可以避免颗粒沉降,并允许具有不同粒径的颗粒以相同速度通过检测池。A Mastersizer 3000粒度分析仪(英国伍斯特郡Malvern仪器有限公司)配有桨式搅拌器和内部超声辅助分散装置。设备的瓦数可以调整到10个等级。在本研究中,设置不同的搅拌器速度(500 – 3500 r/min)和超声强度(0% – 100%)进行研究。计算d (0.1) 、d (0.5) 、d (0.9) 、d (4,3) 、RSD %和残差的平均值。表2、图1C和1D提供了测量结果(如补充数据附录D所示)。
结果表明,搅拌速度对粒径分布有明显的影响。当搅拌器速度大于3000 r/min时,产生气泡,导致结果不准确。搅拌速度为500~2500 r/min时,无明显差异。在搅拌器速度为2500 r/min时获得最佳值。
此外,结果表明,必须采用超声处理来帮助分散颗粒。当超声强度在10% ~ 60%范围内时,未观察到对测量结果的显著影响。但是当超声处理强度大于80%时,测量结果的精度较差。这种现象可能是由于声处理产生的机械能,其可以破坏原始粒子。因此,选择40%的超声强度作为最佳超声强度。
考虑到固定的40%声处理强度没有发生变化,我们研究了不同的声处理时间(0-120秒)对测量结果的影响。结果表明,超声处理时间对颗粒尺寸没有显著影响。最佳超声处理时间设定为60s。
3.5方法验证
在准确度、精密度和重复性方面进行了方法验证。测定各试样,计数d (0.1)、d(0.5)、d (0.9)、d (4,3)的结果。计算平均值、RSD %和加权残差%值。表3提供了结果(如补充数据附录E所示)。
采用已知的d (0.1)、d (0.5)和d (0.9) 标准粒子重复三次验证仪器和方法。根据ISO13320-1(第6.4节),d(0.1)和d(0.9)的观测值和理论值的偏差应小于5%,d(0.5)的偏差应小于3%。如果颗粒尺寸< 10 um,则最大偏差应加倍。平行测量的RSD %值< 3%。结果表明,仪器测量的精度符合要求。
重复测量样品10次。10倍测量的RSD %值< 3%。根据仪器参数和方法制备了5个样品。每个样品重复测量三次。测得的RSD %值结果< 3%。这些结果表明,该方法具有良好的精密度和重复性。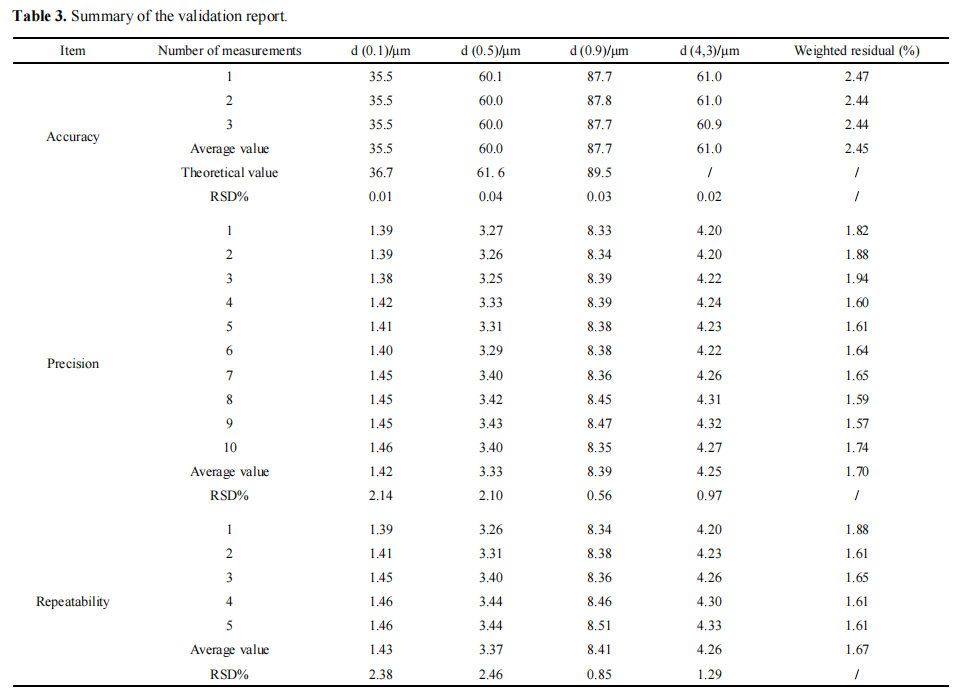
3.6样品粒度测量结果
根据仪器参数和方法制备了四批地拉罗司API样品用于粒度测量。表4显示了结果(补充F)。地拉罗司原料药的粒度和分布的测量结果在两个批次(即20180201和20180203)之间几乎没有差异。平均粒径d(4,3) 约为4μm。批次20180202的粒度相对较大,d(4,3)的平均粒度约为7um。相比之下,批次20190523较小,d值约为2um(4.3)。RSD值< 5%。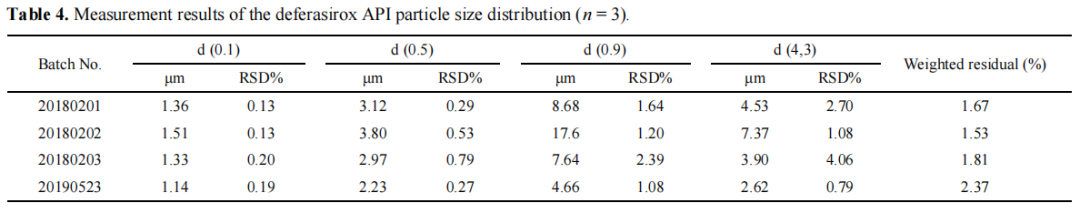
3.7原料药粒度与制剂溶出曲线的相关性
对于具有不同粒度的三批地拉罗司原料药(批号20180201、20180202和20190523),参考列出的参比药物(Exjade®)的配制和技术。制备三个批次(批号20180622、20180629和20191209)的地拉罗司分散片,并将其溶出曲线与列出的参比药物(Exjade ®,批号SP168)在四种溶解介质中。结果表明,地拉罗司原料药的粒径和分布对片剂的体外溶出释放有显著影响。使用大粒径API制备的分散片的溶出速率和累积释放百分比低于使用小粒径API制备的片剂的溶出速率和累积释放百分比,特别是在酸性溶出介质中。在pH 1.0的溶出介质中,分散片20180629(原料药的平均粒径为7um)、20180622(原料药的平均粒径为4μm)和20191209(原料药的平均粒径为2um)5min的溶出速率分别为11.72%、18.18%和分别为21.97%、16.10%、22.12%和26.51%。15 min后溶出曲线趋于平缓,45 min的累积释放百分率分别为18.59%、25.23%和28.40%。在pH 6.8的溶解介质中,可分散的批次20180622、20180629和20191209的片剂基本一致,15min后超过85%。然而,批次20191209中分散片的溶出速率相对较快,即15分钟后溶出速率为97.57%。相比之下,批次20180629仅为89.82%。批次20180622(原料药的平均粒径为4μm)分散片的溶出曲线与参比列出的药物(Exjade ®,批号SP168)。相似因子f2的值>50。图2给出了具体溶出实验结果(如补充数据附录G所示)。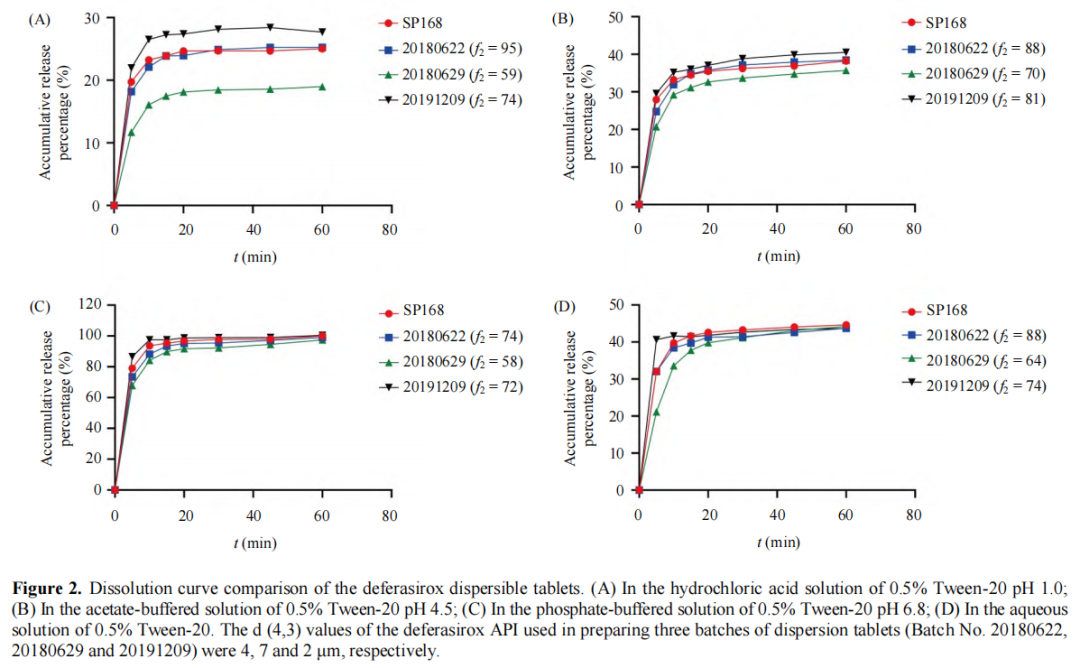
本文采用Mastersizer 3000激光衍射粒度分析仪对地拉罗司原料药的粒度和分布进行了系统的研究。建立了激光衍射法,通过考察重要的光学参数、样品分散条件、分散剂的种类和浓度等关键因素,确定了地拉罗司原料药的粒径。该方法也得到验证。该方法快速、准确、操作简单,重复性好。比较了不同粒径地拉罗司在4种溶出介质中制备的几批分散片的溶出曲线,考察了粒径对药物体外溶出的影响。实验数据显示活性成分在酸性环境中的粒度对地拉罗司分散片的释放产生显著影响。
因此,应建立准确、有效的原料药粒度测定方法,并严格控制原料药粒度,保证药效。
在这个案例研究中,我们提出激光衍射作为评估地拉罗克斯粒子的尺寸和分布的有用工具。这种方法有助于深入理解颗粒特性和药物释放之间的关系。激光衍射提供了寻找最佳粒度分布以确定适当工艺参数的基础。该方法弥补了原药物测定方法的不足,提高了药物质量控制,进一步保证了效率。采用激光衍射作为分析技术在地拉罗司分散片生产过程中,采用设计质量方法。该方法适用于相对直接的质量控制。
略